Investigadores de la UMA desarrollan un método para el diagnóstico del Alzheimer
 1
/
1
1
/
1
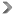
Basadas en conceptos de inteligencia artificial, las técnicas desarrolladas en colaboración con la UGR pueden aplicarse a otras enfermedades como el Parkinson
Categoría: portada
El alzhéimer, que actualmente afecta a más de 40 millones de personas, es la enfermedad neurodegenerativa más común en gente mayor. El diagnóstico temprano resulta crucial tanto para tratar la enfermedad como para ayudar al desarrollo de nuevas medicinas, ya que hasta el momento no ha sido posible encontrar una cura. El desarrollo del alzhéimer ha demostrado estar muy relacionado con cambios tanto estructurales –relacionados con la sustancia gris, encargada del procesamiento de la información– como funcionales –de la sustancia blanca, que conecta las diferentes regiones del cerebro mediante fibras– en la red de conectividad cerebral, puesto que una pérdida significativa de fibras originan también alternaciones funcionales, como la pérdida de memoria. Sin embargo, la diagnosis continúa siendo un reto a pesar de los avances científicos conseguidos y hasta el momento no se ha logrado determinar cómo la actividad cerebral funcional deteriora la estructural y viceversa, lo cual es un elemento clave para comprender mejor el desarrollo de este tipo de enfermedades.
A este respecto, los diagnósticos asistidos por ordenador (DAO) suponen una importante herramienta para el diagnóstico al ayudar a los médicos a interpretar los contenidos multimedia obtenidos en pruebas a los pacientes, lo que permite que la aplicación del tratamiento pueda ser más simple y efectiva. Uno de estos procedimientos son las imágenes médicas, que proporcionan información “en vivo” de gran resolución sobre las materias a estudiar y permiten utilizar la información relacionada con la enfermedad contenida en la imagen. El grupo de trabajo BioSip de la Universidad de Málaga, en colaboración con un grupo de investigadores de la Universidad de Granada, lleva años estudiando las señales e imágenes biomédicas.
Los investigadores Andrés Ortiz, Jorge Munilla, Juan Górriz y Javier Ramírez han publicado recientemente en esta misma línea el artículo “Ensembles of Deep Learning Architectures for the Early Diagnosis of the Alzheimer’s Disease” en la prestigiosa revista International Journal of Neural Systems. Dicho estudio presenta un método para el diagnóstico del alzhéimer mediante la fusión de imágenes funcionales y estructurales basado en el uso de la técnica de aprendizaje profundo –conocido también como Deep Learning–. Esta técnica de la Inteligencia Artificial (IA) tiene como objetivo modelar abstracciones de alto nivel en datos para lograr que las computadoras aprendan a diferenciar el cerebro de una persona sana del de una persona enferma extrayendo automáticamente las regiones de interés que se encuentren afectadas. Como explica el doctor Ortiz, “el estudio utiliza técnicas de aprendizaje profundo para calcular predictores sobre imágenes de funcionalidad cerebral y de resonancia magnética para prevenir la enfermedad de Alzheimer. Para ello, hemos utilizado redes neuronales diferentes con las que modelar cada región del cerebro para posteriormente combinarlas”.
El estudio explora la construcción de métodos de clasificación basados en las arquitecturas de Deep Learning aplicadas a regiones cerebrales definidas por el Automated Anatomical Labeling (AAL), un altas digital del cerebro humano. Para ello, se han dividido las imágenes de la materia gris de cada área del cerebro de acuerdo a las regiones divididas por el AAL en diferentes sectores que se han utilizado para entrenar redes neuronales de Deep Learning especializadas en las distintas regiones del cerebro. El conocimiento adquirido por dichas redes se combina posteriormente mediante diferentes técnicas de fusión que se presentan en este trabajo.
El resultado de este trabajo es una potente arquitectura de clasificación que combina el aprendizaje supervisado y no supervisado para extraer de forma automática las características más relevantes de un conjunto de imágenes. El método propuesto ha sido evaluado utilizando una enorme base de datos provenientes del Alzheimer’s Disease Neuroimaging Initative (ADNI).
Los resultados de este trabajo, que además ha incluido a pacientes de otras deficiencias cognitivas que pueden desarrollar alzhéimer en un plazo de dos años, muestran la potencialidad de las técnicas de IA para revelar los patrones asociados a la enfermedad. Las tasas de precisión obtenidas para el diagnóstico permiten dar un gran paso en el conocimiento del proceso neurodegenerativo implicado en el desarrollo de la enfermedad, además de servir de punto de partida para el desarrollo de tratamientos médicos más efectivos.
Por otro lado, las técnicas desarrolladas pueden servir o ser punto de partida para la mejora de la precisión en el diagnóstico de otras demencias como la enfermedad de Parkinson, donde también trabaja el grupo BioSip. Además, los métodos desarrollados se están utilizando en la mejora del diagnóstico y en la investigación del origen biológico de dificultades de aprendizaje como la dislexia, en un proyecto financiado por el Ministerio de Economía y Competitividad en el que participan los investigadores del grupo junto con investigadores del grupo Leeduca de la Universidad de Málaga.
05-10- 2016
Andrés Ortiz, Jorge Munilla, Juan M. Górriz y Javier Ramírez. "Ensembles of deep learning architectures for the early diagnosis of alzheimer's disease". International Journal of Neural Systems. Volume 26, Issue 07. Disponible en línea: http://dx.doi.org/10.1142/S0129065716500258





